(1)镀液中铜离子的络合状态 焦磷酸盐镀铜液是络盐型镀液之一。它主要是利用焦磷酸钾可将供给铜离子的焦磷酸铜络合而生成焦磷酸铜钾这样一种螯合物。 焦磷酸铜难溶解于水,但能溶解在焦磷酸钾溶液中,形成焦磷酸铜钾: Cu2P207+3K4P207—2K6[Cu(P207)2] 铜离子与焦磷酸组成的络合盐在不同的pH值下有着不同的形式:当pH<5.3时,可能存在的主要形式为[CuH2(P207)2]4-;当pH值为5.3~7时,主要形式为[Cull(P2 07)2]5-;当pH值为7~10时,主要以[Cu(P207)2]6‑形式存在。由此可知,焦磷酸镀铜溶液的pH值对络离子的存在形式影响很大,考虑到pH≥8.5时,镀液中主要以[CuP207)2]6-形式存在,而这种形式的离子所带的负电荷数比其他形式的络离子要多,对阴极过程影响也大。 所以镀液的pH值宜控制在8.5~9之间较合适。生产实践证明了在这种pH值范围内所获得的镀层质量最好,结晶细致,深镀能力和分散能力都比较好。 (2)[Cu(P207)2]6-的不稳定常数 在pH值7~10的范围内,焦磷酸铜钾的水溶液中存在着如下的离子平衡:
而[Cu(P207)2]6-络离子也存在着一个离子平衡:
其不稳定常数为:
由于焦磷酸与铜离子的络合能力远比氰化物与铜离子交换的络合能力差([Cu+][CN-]3/[Cu(CN)3]2-)一2.6×10-2g),为了使[Cu(P207)2]6-络合离子更稳定,镀液中应有大量的焦磷酸钾(俗称游离焦磷酸根),以防止焦磷酸铜沉淀。同时,过量的焦磷酸钾还可改善镀层结晶状态,提高镀液的分散能力,并使阳极正常溶解。 (3)主要的电极反应 ①镀液中的离子状态。首先,K6[Cu(P207)2]分解为:
接着, [Cu(P207)2]6-络离子在阴极双电层区按下式分解:
或
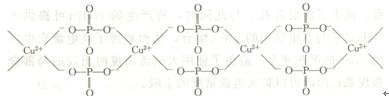
②阴极反应。对于[Cu(P2O2)2]6-络离子来说,它在阴极上直接放电是比较困难的,因为它有较高的配位数和较多的负电荷数,估计在阴极上放电的是[Cu(P207)]2-络离子: [Cu(P207)]2-+2e→Cu+P2O74- 这样的反应步骤之所以能成立是因为[Cu(P207)]2一络离子的半径比[Cu(P207)2]6一络离子小,配位数低,相应地在电极上放电所需要的活化能也较低,受荷负电的电极的排斥作用弱一些,而且从[Cu(P207)2]6一络离子转化为[Cu(P207)]2一络离子的速度不够快,这一步是提高阴极极化的主要因素之一。 在阴极上起副反应的还有: Cu2++2e—→Cu 2H++2e—H2↑ 2H20+2e—H2↑+20H一 由于焦磷酸盐镀铜的电流效率接近100%,这表明H+很少放电。 如果溶液中有NOr存在,则还进行如下反应: NO3-+7H20+8e—NH4++100H— NO3-+10H++8e—NH4++3H20 由于上述反应是消耗H+的,从而抑制了H+的还原过程,减少了镀层针孔。与此同时,所产生的NH3+可提供出NH3,它与双电层中的Cu2+络合,从而减慢了高电流密度区的Cu2+的沉积速度,避免了使用大电流密度时出现的局部烧焦现象;因而可以扩大电流密度的上限。 难怪在焦磷酸盐镀铜体系中,NO3-不作为有害杂质,相反,还有人引进15~20g/L硝酸钾或硝酸铵作为辅助导电盐。正因为焦磷酸盐镀铜致密,孑L隙少,难怪许多电子元件和要求耐蚀高的功能性电镀都要求焦磷酸盐镀铜这一镀层。 ③阳极反应。由于焦磷酸盐镀铜溶液中含有P2074一、OH一、C6H50一和HPO42-等多种阴离子,其中有的阴离子对金属阳极溶解起到活化作用,有的因相互影响起到阻化效应,所以阴离子对阳极过程将起到复杂的作用。 焦磷酸盐镀铜时,阳极上的主要反应是金属铜失去电子变成2价铜离子进入溶液,并与溶液中的游离焦磷酸根反应生成铜络离子。 Cu一2e→Cu2+ Cu2++2P2074—→[Cu(P207)2]6- 阴离子也可直接参加电极反应: Cu+2P2074—一2e→[Cu(P207)2]6- 当阳极发生钝化时,阳极还有氧气放出,其反应式如下: 40H一一4e→2H20+02↑ 当然,对于复杂体系的焦磷酸盐镀铜溶液来源,阳极的溶解过程不会这样简单,实际上,柠檬酸根等阴离子也参与了阳极反应,试验表明,柠檬酸根有较好的去阳极极化作用。 至于引起阳极钝化的原因,还会受到阳极电流密度、pH值、温度等工艺参数以及配体性质的影响。有人认为:焦磷酸镀铜溶液之所以常引起阳极钝化,有可能是P2074—和Cu2+形成大分子链状络合物有关:
这种链状络合物的扩散速度很小,使溶解下来的Cu2+不易离开阳极,造成阳极附近的Cu2+浓度增大,使金属不易连续溶解下来。此时,它易与氧结合而生成氧化膜,致使阳极钝化。所以镀铜时要求搅拌溶液,这对阳极的溶解有好处。 |