|
关 键 词:化学镀镍,废水,化学沉淀,镍回收 作 者:施银燕,徐玉福,胡献国 内 容: (合肥工业大学机械与汽车工程学院,安徽合肥230009) 摘要:采用化学沉淀法从化学镀镍废水中回收镍,通过实验优化了NaOH处理含镍废水的工艺参数,并对沉渣镍盐进行了处理。结果表明,化学沉淀法处理化学镀镍废水的最佳工艺参数为:H2O2 30 mL/L,NaOH 15.67 g/L,絮凝剂聚丙烯酰胺4 g/L。用硫酸处理沉淀物后镍的回收率可达97.25%。 关键词:化学镀镍,废水,化学沉淀,镍回收 中图分类号:X 781.1 文献标识码:A 文章编号:1000-4742(2011)05-0044-03 O前言 化学镀镍是以镍盐和次磷酸盐等作用生成Ni-P非晶镀层[1],具有不需外电源、镀层均匀、硬度高、耐磨性能好、镀覆部件不受尺寸形状限制等优点,已经广泛应用于机械零件的耐磨与减摩以及表面强化等领域。但目前大部分化学镀镍废水以废水的形式直接排放,造成资源浪费。同时镍的毒性较大,含镍废水直接排放必将对环境和人体健康造成危害[2-3]。因此,研究化学镀镍废水中Ni2+的回收利用方法已引起国内外广泛关注。 目前化学镀镍废水的处理方法有很多,如电解法、化学法、吸附法、生物法等。其中化学沉淀法简便、实用,在含镍废水处理中应用最多,且随着在线监测自动控制仪的使用,有逐渐增加的趋势。由于化学镀镍废水的化学成分复杂,配位剂的质量浓度高,难以直接用沉淀的方法彻底回收镍。本文用破配位剂首先破坏化学镀镍废水的配位能力,进而以 NaOH为沉淀剂,最大程度地回收化学镀镍废水中的镍。 1 实验 1.1 废水成分分析 本实验所用化学镀镍废水取自某金属材料公司,经过滤处理后,废水的pH值为4.30,主要成分为:Ni2+17367 mg/L,Fe2+3.O mg/L,Cu2+15.2 mg/L,Zn2+13.7 mg/L。 由以上水质数据可知:该公司排放的含镍废水中,Ni2+的质量浓度很高,回收其中的Ni2+不仅可以减小对环境的污染,更有利于提高企业的经济效益。 1.2主要仪器及试剂 采用的主要仪器有721分光光度计,pH计。采用的主要试剂有NaOH( AR),质量分数为30%的H2O2。 1.3 实验方法 (1)废水成分分析 取经过过滤除杂的含镍废水,用原子吸收光谱分析法分析溶液中的离子组成。 (2)废水处理 向废水中加入一定量的H2O2进行破配位处理,然后加入一定量的NaOH搅拌0.5 h,静置分层,测定上层清液中的Ni2+的质量浓度,计算Ni2+的去除率。 (3)聚丙烯酰胺(PAM)对沉淀速率的影响 取100 mL废水,向废水中加入30 mL/L的 H2O2,常温下再向废水中加入15.67 g/L的固体 NaOH和一定量的PAM,反应0.5 h后立即转入到带有刻度的试管中,记录沉淀物沉淀至40 mL处时的时间,考察PAM的质量浓度对沉淀速率的影响。 (4)沉淀物的处理 取100 mL废水,向废水中加入30 mL/L的H2O2,常温下再向废水中加入15.67 g/L的固体 NaOH和一定量的PAM,反应0.5 h后过滤,将滤饼置于烘箱中于120℃下干燥2h,称重。然后将 Ni (OH)2用0.1 mol/L的H2S04溶解,蒸发结晶,得到镍的硫酸盐,称重,计算镍的回收率。 2 结果与讨论 2.1 H2O2对Ni2+去除率的影响 向100 mL废水中加入一定量的H2O2,然后加入1.5 g NaOH,搅拌0.5 h,实验结果,如图1所示。 由图1可知:在废水中加入H2O2,Ni2+的去除效率明显提高,且随着H2O2的体积分数的增加, Ni2+去除率也增加。这是因为在化学镀镍废水中镍主要以配位物[Ni3(C6H5O7)2]的形式存在,只靠加碱很难使镍沉淀完全。加入H2O2可以破坏配位物[4],形成更多的游离Ni2+,使得Ni2+的去除率提高。从图中还可以看出:当H2O2的体积分数达到30 mL/L后,去除率不再增加。由此可见,H2O2最佳体积分数为30 mL/L。 2.2 NaOH对废水pH值的影响 向废水中加入30 mL/L的H2O2,常温下,缓慢添加不同质量浓度的NaOH,同时测定反应体系的 pH值,实验结果,如图2所示。
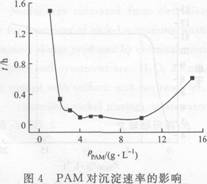
由图2可知:当NaOH的质量浓度在3.79 g/L以内时,反应体系的pH值随着NaOH的质量浓度的增加迅速增加,这是因为添加的NaOH与废水中的H+反应,导致pH值迅速上升;当NaOH的质量浓度达到3.79 g/L后,体系的pH值达到11.26,继 续添加NaOH,pH值不再变化,这是因为OH-与废水中的Ni2+发生反应,生成Ni(OH)2,pH值不 变化;而当NaOH的质量浓度达到15.67 g/L后,废水的pH值开始上升,这时Ni2+沉淀完全,继续 添加的OH-会导致废水pH上升。因此,NaOH的最佳质量浓度为15.67 g/L,此时能确保废水中 Ni2+沉淀完全。 2.3 NaOH对Ni2+去除率的影响 向废水中加入30 mL/L的H2O2,常温下,缓慢添加不同质量浓度的NaOH,并搅拌0.5 h,测定反应体系Ni2+的去除率,实验结果,如图3所示。 由图3可知:Ni2+的去除率随着NaOH的质量浓度的增加而上升,当其质量浓度达到15.67 g/L后,Ni2+的去除率不再变化,此时pH值也开始上升,如图2所示。因此,为使Ni2+的去除率最大, NaOH的质量浓度应达到15.67 g/L。 2.4 PAM对沉淀速率的影响 在处理过程中加入一定量的PAM,测定其对沉淀速率的影响,实验结果,如图4所示。 由于反应生成的Ni(OH)2粒度很小,沉淀速率很慢,在不加入絮凝剂的情况下沉淀至40 mL处需要3天左右。由图4可知:加入PAM后,沉淀速率迅速提高。这是因为在PAM絮凝过程中,当悬浮微粒的质量浓度较低时,吸附在PAM表面上的悬浮微粒可能同时吸附在另一个微粒的表面上,通过“架桥”方式将两个或更多的微粒连在一起,从而导致絮凝[5]。当PAM的质量浓度达到4 g/L后,沉淀速率趋于平缓。尽管从图中可以看出:当PAM的质量浓度为10 g/L时,沉淀所需时间最少,但考虑到成本问题,PAM的质量浓度取4 g/L为宜。同时从图中可以看出:当PAM的质量浓度超过10 g/L后,沉淀时间变长,絮凝效果降低。这是因为 PAM过量时,“架桥”作用所必需的粒子表面吸附活性点少了,“架桥”因而变得困难;同时,由于粒子间的相互排斥作用而出现分散稳定现象[6]。 2.5镍沉淀的处理 100 mL废水处理后产生的Ni(OH)2沉淀为2.7539 g,Ni2+的回收率为99.97%。硫酸溶解后,蒸发结晶,得到NiSO4·7H2O的质量为7.6297 g,Ni2+的回收率为97.28%。故废水中镍的总回收率=99.97%×97.28%=97.25%。因此使用该工艺可以很大程度地解决含镍废水的污染问题,同时可以回收大量的镍,减少了资源浪费,也能给企业带来一定的经济效益。 3 结论 化学镀镍废水中Ni2+的质量浓度高,废液中含有大量的有机配位剂和添加剂,镍主要以配位物的形式存在。化学沉淀法处理化学镀镍废水的最佳工艺参数为:H2O2 30 mL/L,NaOH 15.67 g/L,PAM4 g/L,在室温下搅拌0.5 h。此时,Ni2+的去除率最佳。沉淀物用稀硫酸溶解回收镍盐,镍的回收率可达到97.25%。 参考文献: [1]陈志勇,王辉,漂白粉氧化处理化学镀镍废液的研究[J].电镀与环保,2001,21(4):30-31. [2]王学锋,术桂芬。重金属污染研究新进展[J].环境科学与技术, 2003,26(1):54-56. [3]盂祥和,胡国飞,重金属废水处理[M].北京:化学工业出版社, 2000:5-12. [4]王晓波,萨如拉,杨润昌,等,化学镀镍废液处理新工艺及机理研究[J].湘潭大学自然科学学报,2004,26(1):78-80. [5]湛含辉,钟乐,韦小利,聚丙烯酰胺絮凝机理及流体力化学因素的研究[Jl.选煤技术,2007(1):7-11. [6]刘军,聚丙烯酰胺在工业废水处理中的应用[J].广西轻化工, 2009(7):98-99. 注:本站部分资料需要安装PDF阅读器才能查看,如果你不能浏览文章全文,请检查你是否已安装PDF阅读器! |